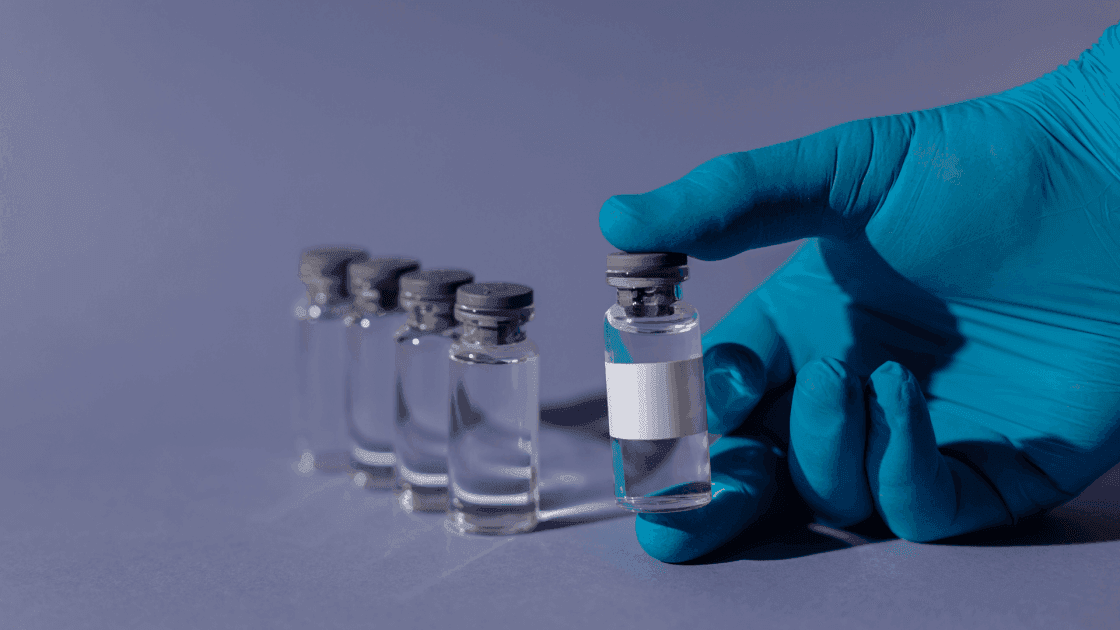
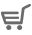Prof. Shoenfeld: “Gli adiuvanti dei vaccini hanno una propensione a scatenare malattie autoimmuni”
Salute e Benessere Naturali

Salute e Benessere Naturali
Il professore Yehuda Shoenfeld (nella foto), immunologo dell’Università di Tel Aviv, studia da anni, insieme a un team di ricercatori di tutto il mondo, gli effetti collaterali degli adiuvanti dei vaccini e in particolare la loro propensione a scatenare malattie autoimmuni. Secondo il prof. Shoenfeld tali adiuvanti presenti nelle composizioni standard dei vaccini inducono in alcuni soggetti predisposti una catena di effetti nocivi che porta a sviluppare nel tempo patologie anche gravi e debilitanti come lupus eritematoso sistemico, fibromialgia, stanchezza cronica, neuropatie, sclerosi multipla, vascuiliti, disordini reumatici autoimmuni, miastenia, artriti, mieliti, miopatie ecc.
Valerio Pignatta
Un concetto base che viene fuori da queste ricerche è quello di diversità biologica di ogni individuo che appunto in natura non è mai identico a un altro. È un principio molto logico e di cui la medicina dovrebbe avere imparato a tener conto, ma di fatto ancora non esiste una medicina personalizzata, seppure se ne inizia a sentir parlare. Per certo, somministrare a tutta la popolazione, in campagne vaccinali di massa, lo stesso vaccino aspettandosi gli stessi risultati in ogni individuo è alquanto irrazionale secondo le più recenti (e comunque neanche tanto) acquisizioni della biologia e della fisiologia. Eppure tali trattamenti proseguono senza che nessuna organizzazione o istituzione sanitaria si soffermi a ragionarci sopra.
Il professor Yehuda Shoenfeld autore del libro Vaccini a Autoimmunità

La variabilità delle risposte vaccinali rimane una caratteristica complessa
Come riportano i membri del gruppo di Shoenfeld, in un ultimo loro lavoro, si dovrebbe invece tener conto che «la variabilità delle risposte vaccinali tra diversi individui rimane una caratteristica complessa che richiede ulteriori indagini, poiché un'alta percentuale di individui vaccinati non ha una protezione completa dopo le vaccinazioni di routine (ad esempio il 10-15% degli adulti non risponde a tre dosi di vaccino del virus dell'epatite B [HBV]) (Roome et al., 1993)».
Ma si possono fare altri esempi, come quello del vaccino MPR, le risposte al quale pure variano da individuo a individuo: «I vaccini, come quello per morbillo, parotite e rosolia (MPR) [...] non riescono a indurre livelli di anticorpi protettivi a vita in circa il 5-10% dei destinatari sani. Per questo motivo, continuano a manifestarsi epidemie in tutto il mondo (Poland e Jacobson, 1994)».
Allo stesso modo, gli individui reagiscono differentemente agli adiuvanti contenuti nei vaccini stessi. In percentuali che variano da vaccino a vaccino ci sono pazienti che sviluppano malattie autoimmuni in conseguenza degli stessi. Per farci un’idea, possiamo prendere il caso delle correlazioni tra vaccino antiepatite B e neuropatie. Afferma il team di Shoenfeld: «Ad oggi non ci sono prove conclusive che colleghino il vaccino HBV alla neuropatia (Stubgen, 2010).
Scopri la più importante ricerca scientifica sui vaccini!
Tuttavia, diversi casi riportano lo sviluppo di neuropatia (comprese molte sindromi di Guillain-Barré [GBS]) dopo il vaccino HBV ricombinante e plasma-derivato (Tuohy, 1989; McMahon et al., 1992; Kakar e Sethi, 1997; Maillefert et al., 1997; Creange et al., 1999; Sinsawaiwong e Thampanitchawong, 2000; Dano e Korczyn, 2001; DeJonckere e de Surgeres, 2001; Sindern et al., 2001; Seti et al., 2002; Khamaisi et al., 2004).
Il numero di inoculazioni prima dello sviluppo dei sintomi variava da uno a quattro, con un tempo tra l'iniezione e l'insorgenza dei sintomi compreso tra 1 giorno e 8 settimane (Tuohy, 1989; McMahon et al., 1992; Kakar e Sethi, 1997; Maillefert et al., 1997; Creange et al., 1999; Sinsawaiwong e Thampanitchawong, 2000; Dano e Korczyn, 2001; DeJonckere e de Surgeres, 2001; Sindern et al., 2001; Seti et al., 2002; Khamaisi et al., 2004).
Oltre ai casi clinici, la sorveglianza post-marketing dopo somministrazione del vaccino HBV in 850.000 pazienti ha rivelato eventi neurologici multipli, tra cui cinque casi di convulsioni, dieci paralisi di Bell, nove GBS, cinque radicolopatie lombari, tre neuropatie del plesso brachiale, cinque neuriti ottiche e quattro mieliti trasverse (Shaw et al., 1988). Ulteriori studi che hanno utilizzato il VAERS [Vaccine Adverse Event Reporting System] hanno anche rilevato che il vaccino HBV è legato a eventi di autoimmunità, tra cui GBS (Geier e Geier, 2004; Haber et al., 2004; Souayah et al., 2009; van Doorn, 2009)».
Da questi dati si evince che la questione è molto complessa e che la medicina ha tutt’altro che sotto controllo ciò che avviene con la vaccinazione. I ricercatori infatti suggeriscono infine che: «È chiaro che sono necessarie ulteriori ricerche per identificare gli individui che potrebbero sviluppare malattie autoimmuni in seguito a vaccinazioni. Sebbene predisposizione genetica e storia personale e familiare di autoimmunità rappresentino chiari fattori di rischio, abbiamo notato con interesse che il 57% delle segnalazioni di casi di autoimmunità nella letteratura attualmente disponibile non aveva tale suscettibilità. Pertanto, ulteriori indagini dovrebbero mirare ad identificare altri fattori di rischio, che possono includere precedenti esposizioni a farmaci (inclusi contraccettivi orali, altre vaccinazioni, farmaci antipsicotici, fumo ecc.)» (Shoenfeld et al., 2015).
Bibliografia
Creange, A., Temam, G. e Lefaucheur, J.P. (1999). Lumbosacral acute demyelinating polyneuropathy following hepatitis B vaccination. Autoimmunity, 30(3): 143–6.
Dano, M. e Korczyn, A.D. (2001). Precipitation of hereditary motor-sensory neuropathy following hepatitis B vaccination. J Clin Neuromuscul Dis, 3(2): 75–6.
DeJonckere e de Surgeres, 2001; DeJonckere, P.H. e de Surgeres, G.G. (2001). Acute tinnitus and permanent audiovestibular damage after hepatitis B vaccination. Int Tinnitus J, 7(1): 59–61.
Geier, M.R. e Geier, D.A. (2004). A case-series of adverse events, positive re-challenge of symptoms, and events in identical twins following hepatitis B vaccination: analysis of the Vaccine Adverse Event Reporting System (VAERS) database and literature review. Clin Exp Rheumatol, 22(6): 749–55.
Haber, P., DeStefano, F., Angulo, F.J., et al. (2004). Guillain-Barre syndrome following influenza vaccination. JAMA, 292(20): 2478–81.
Kakar, A. e Sethi, P.K. (1997). Guillain Barre syndrome associated with hepatitis B vaccination. Indian J Pediatr, 64(5): 710–12.
Khamaisi, M., Shoenfeld, Y. e Orbach, H. (2004). Guillain-Barre syndrome following hepatitis B vaccination. Clin Exp Rheumatol, 22(6): 767–70.
Maillefert, J.F., Farge, P., Gazet-Maillefert, M.P. e Tavernier, C. (1997). Mental nerve neuropathy as a result of hepatitis B vaccination. Oral Surg Oral Med Oral Pathol Oral Radiol Endod, 83(6): 663–4.
McMahon, B.J., Helminiak, C., Wainwright, R.B., et al. (1992). Frequency of adverse reactions to hepatitis B vaccine in 43,618 persons. Am J Med, 92(3): 254–6.
Poland, G.A. e Jacobson, R.M. (1994). Failure to reach the goal of measles elimination. Apparent paradox of measles infections in immunized persons. Arch Intern Med, 154(16): 1815–20
Roome, A.J., Walsh, S.J., Cartter, M.L. e Hadler, J.L. (1993). Hepatitis B vaccine responsiveness in Connecticut public safety personnel. JAMA, 270 (24), 2931–4.
Seti, N.K., Reddi, R., Anand, I. e Sethi, P.K. (2002). Gulliane Barre syndrome following vaccination with hepatitis B vaccine. J Assoc Physicians India, 50: 989.
Shaw, F.E. Jr, Graham, D.J., Guess, H.A., et al. (1988). Postmarketing surveillance for neurologic adverse events reported after hepatitis B vaccination. Experience of the first three years. Am J Epidemiol, 127(2): 337–52.
Shoenfeld, Y., Agmon-Levin, N., Tomljenovic, L., (2015), Vaccine and autoimmunity, Wiley, Hoboken, 171.
Sindern, E., Schroder, J.M., Krismann, M. e Malin, J.P. (2001). Inflammatory polyradiculoneuropathy with spinal cord involvement and lethal [correction of letal] outcome after hepatitis B vaccination. J Neurol Sci, 186(1–2): 81–5.
Sinsawaiwong, S. e Thampanitchawong, P. (2000). Guillain–Barré syndrome following recombinant hepatitis B vaccine and literature review. J Med Assoc Thai, 83(9): 1124–6.
Souayah, N., Nasar, A., Suri, M.F. e Qureshi, A.I. (2009). Guillain-Barre syndrome after vaccination in United States: data from the Centers for Disease Control and Prevention/Food and Drug Administration Vaccine Adverse Event Reporting System (1990–2005). J Clin Neuromuscul Dis, 11(1): 1–6.
Stubgen, J.P. (2010). Neuromuscular disorders associated with Hepatitis B vaccination. J Neurol Sci, 292(1–2): 1–4.
Tuohy, P.G. (1989). Guillain–Barre syndrome following immunisation with synthetic hepatitis B vaccine. N Z Med J, 102(863): 114–15.
van Doorn, P.A. (2009). What’s new in Guillain–Barre syndrome in 2007–2008? J Peripher Nerv Syst, 14(2): 72–4.
Approfondisci l'argomento con il libro Vaccini e Autoimmunità